Все мы знаем из школьного курса физики, что при изменении веществом своего агрегатного состояния происходит фазовый переход. Вещество в твёрдом состоянии может напрямую перейти в газообразное. Например, когда температура сухого льда (твёрдого диоксида углерода, CO2) повышается, он превращается в газ. Этот процесс называется сублимацией или возгонкой.
Но чаще происходят другие процессы. К примеру, когда вода замерзает, из жидкого состояния она переходит в твёрдое (кристаллизация). Когда камни плавятся в лаве, из твёрдого вещества они превращаются в жидкость (плавление). Когда вода закипает в чайнике, из жидкости она становится газом (испарение и кипение). Пока рассматриваемое вещество при подведении или отведении дополнительного тепла переходит в новое состояние – жидкое, твёрдое или газообразное, температура не меняется. Почему так происходит?
| Краткий ответ. Потому что вся поступающая тепловая энергия идет на разрушение связей между молекулами вещества (в случае плавления — на разрушение кристаллической решетки, в случае кипения — на преодоление молекулами сил межмолекулярного притяжение и вылет за пределы жидкости). Наоборот, при обратных фазовых переходах (конденсации и кристаллизации) температура не уменьшается, потому что происходит образование связей между молекулами вещества. |
Подробное объяснение почему при плавлении температура не меняется
Представьте, что вы спокойно пьёте лимонад (который имеет примерно ту же теплоёмкость, что и обычная вода). В этом лимонаде плавают кусочки льда. Температура этой наполовину лимонадной, наполовину ледяной смеси находится вблизи нуля градусов по Цельсию. Пока вы держите в ладонях стакан и наблюдаете за происходящим в нём процессом, лёд начинает таять, однако содержимое ёмкости не нагревается, пока весь лёд в ней не растает.
Вопрос. Почему при плавлении температура не меняется? Тепловая энергия, поступающая из окружающей среды, плавит лёд, не нагревая смесь в целом. Делает ли это уравнение для расчёта количества теплоты (![]() , где
, где ![]() — количество теплоты,
— количество теплоты, ![]() — масса образца,
— масса образца, ![]() — изменение температуры) бесполезным? Вовсе нет – это лишь означает, что оно неприменимо к фазовому переходу.
— изменение температуры) бесполезным? Вовсе нет – это лишь означает, что оно неприменимо к фазовому переходу.
Можно построить график зависимости температуры вещества ![]() от количества переданной теплоты
от количества переданной теплоты ![]() . К примеру, на Рис. 1 представлен график фазовых переходов льда, взятого из морозильной камеры. Участок
. К примеру, на Рис. 1 представлен график фазовых переходов льда, взятого из морозильной камеры. Участок ![]() соответствует нагреванию льда, участок
соответствует нагреванию льда, участок ![]() — плавлению льда, участок
— плавлению льда, участок ![]() — нагреванию получившейся воды, участок
— нагреванию получившейся воды, участок ![]() — кипению воды, участок
— кипению воды, участок ![]() — нагреванию полученного пара.
— нагреванию полученного пара.
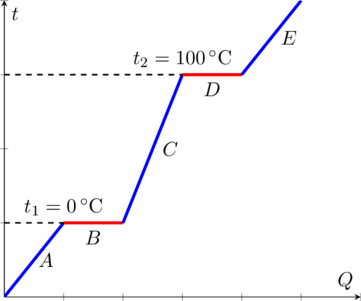
Рис. 1. График фазовых переходов H20.
Как видно, кривая обычно возрастает, то есть увеличение теплоты приводит к возрастанию температуры. Однако кривая идёт горизонтально при фазовых переходах (при температурах ![]() и
и ![]() ), поскольку изменение состояния вещества требует энергии. После того, как переход завершается, температура вновь начинает возрастать.
), поскольку изменение состояния вещества требует энергии. После того, как переход завершается, температура вновь начинает возрастать.
Давайте представим, что вы взяли мешок со льдом и поставил его на кухонную плиту. Перед этим температура льда была ниже температуры замерзания воды, скажем -5 °C. Но на плите она начала изменяться. Пока фазовый переход не происходит, температура льда линейно возрастает при увеличении количества подведенной теплоты ![]() , где c = 2100 Дж/(кг⋅°C) — удельная теплоемкость льда.
, где c = 2100 Дж/(кг⋅°C) — удельная теплоемкость льда.
Когда же лёд достигает температуры в t1 = 0 °C, он становится слишком тёплым, чтобы оставаться в твёрдом состоянии, и начинает плавиться, испытывая фазовый переход (кривая на графике выравнивается). Этот процесс – разрушение кристаллической решётки льда – нуждается в энергии, которая вырабатывается источником тепла. Вот почему при плавлении температура не меняется.
Наблюдая за мешком на плите в течение некоторого времени, вы замечаете, что весь лёд наконец расплавился. Поскольку плита продолжает вырабатывать тепловую энергию, температура воды поднимается. Наконец в ней появляются пузырьки. «Ага, – подумаете вы, – ещё один фазовый переход». Да, это так. Вода становится горячей и при температуре t2 = 100 °C закипает. Мешок при этом начинает раздуваться.
Вы измеряете температуру воды. Удивительно, но пока вода кипит, её температура также не изменяется. И снова, для завершения перехода – из жидкого состояния в газообразное – требуется определённое количество теплоты.
Что же произойдёт дальше, когда мешок расширится до немыслимых размеров? Лучше не проверять, поскольку мешок может взорваться, и вы ошпаритесь горячим паром и кипящей водой.


Спасибо, помогло